定量检测质粒残留DNA,谁才是稳定准确的最佳选择?
背景概述
质粒是一类存在于细菌和真菌细胞中独立于染色体 DNA 而自主复制的共价、闭合、环状 DNA 分子,通常携带一定数量的基因,是基因工程最常见的载体。
mRNA 药物生产流程包括:种子模板制备、质粒 DNA 发酵、质粒 DNA 纯化、mRNA 合成、mRNA 纯化和 LNP 包封纯化及制剂分装,其中 mRNA 合成是以线性化质粒 DNA 作为模板进行体外转录的,因此,mRNA 原液中可能存在质粒DNA 的残留。
生物制品中质粒残留 DNA 不仅是生产中带来的杂质,还存在一定安全隐患,进入人体后可造成多种多样的后果,具有致癌性,感染性,潜在的重组风险和免疫原性增加等风险。mRNA 生产中应采取措施控制和限制质粒残留 DNA 的含量,包括生产工艺优化、原材料选择和酶切纯化等措施,以确保产品的质量和安全。为监管 mRNA 药物的生产工艺,确保其质量稳定性和安全性,国内外监管机构建立了质粒残留 DNA 的检测标准和检测方法。
瀚海新酶结合灵敏性、特异性与耗时短的特点,采用 qPCR 荧光探针的方法,开发了针对 mRNA 药物中质粒残留 DNA 的检测试剂盒。本试剂盒针对卡那霉素抗性基因设计特异性引物,能够定量检测样品中含有卡那霉素抗性基因的质粒 DNA 残留。
实际样本检测结果




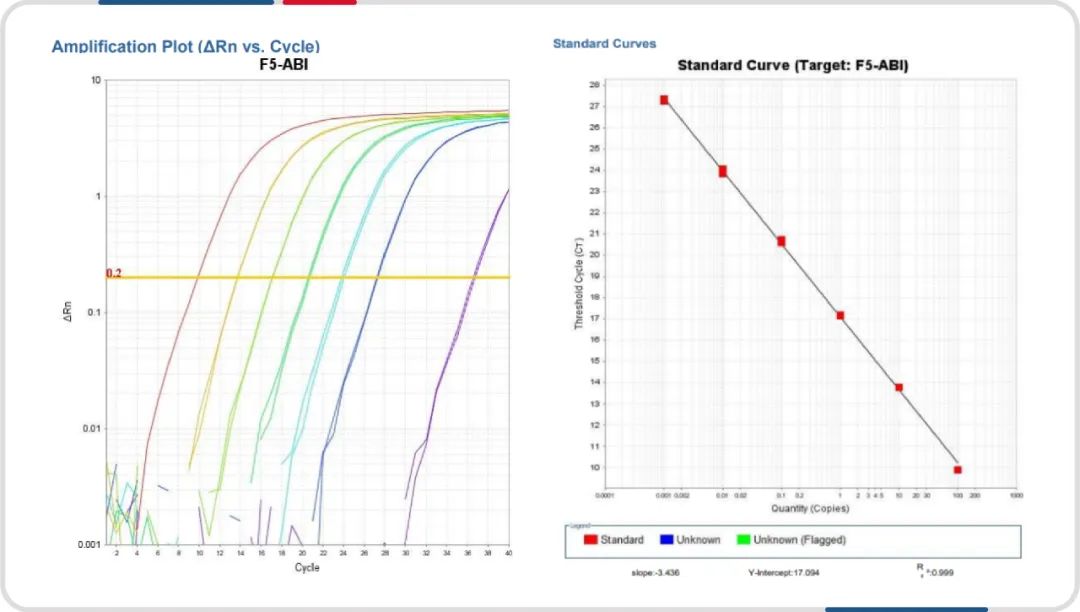
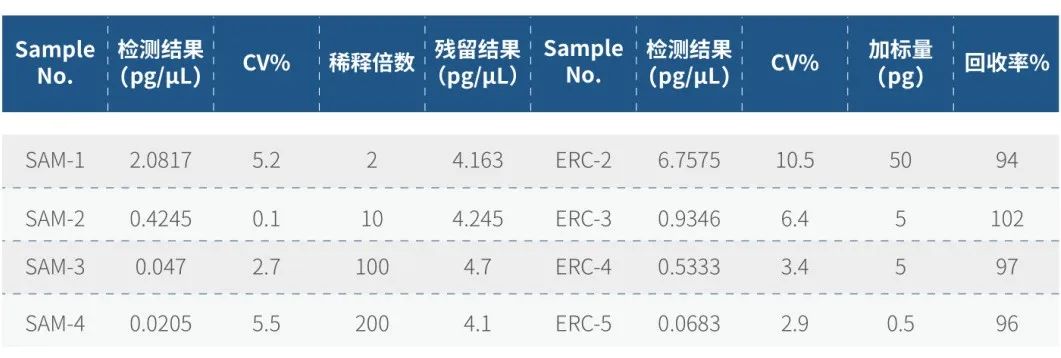
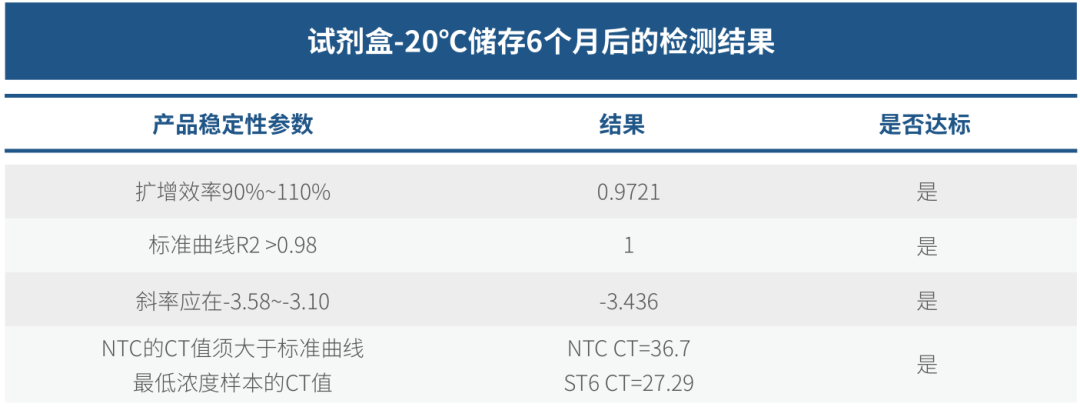











请先 登录后发表评论 ~